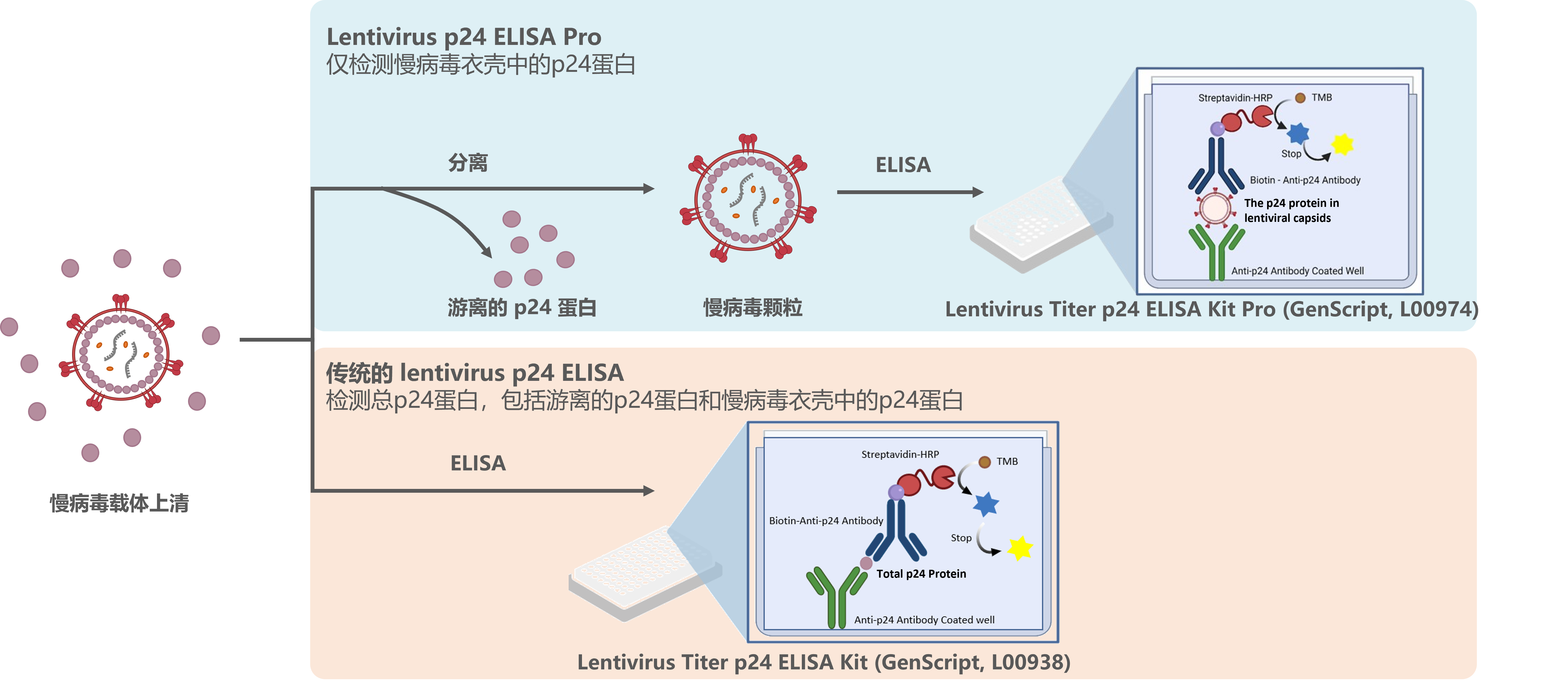
图1:检测原理

| 产品编号 | 名称 | 数量 | 价格 | 操作 |
|---|---|---|---|---|
|
L00938
|
Lentivirus Titer p24 ELISA Kit |
|
¥4980.00 96 Tests |
|
|
L00974
|
Lentivirus Titer p24 ELISA Kit Pro |
|
¥5480.00 96 Tests |
|
|
L01019
|
Lentivirus Titer p24 Kit Easy |
|
¥2590.00 96 Tests |
|

图1:检测原理

图2:检测流程图
Lentivirus Titer p24 ELISA Kit Pro对游离p24的去干扰能力
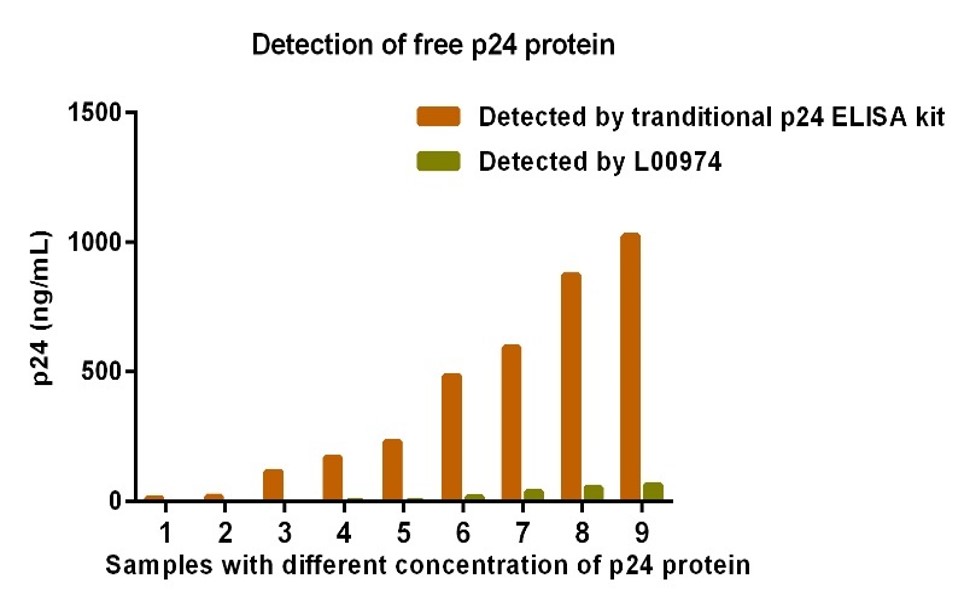
图3:有效减少游离p24的干扰
将不同浓度的p24蛋白添加稀释液中,结果显示,Lentivirus Titer p24 ELISA Kit Pro (GenScript, L00974) 基本不会检测到添加到稀释液中的游离p24蛋白。
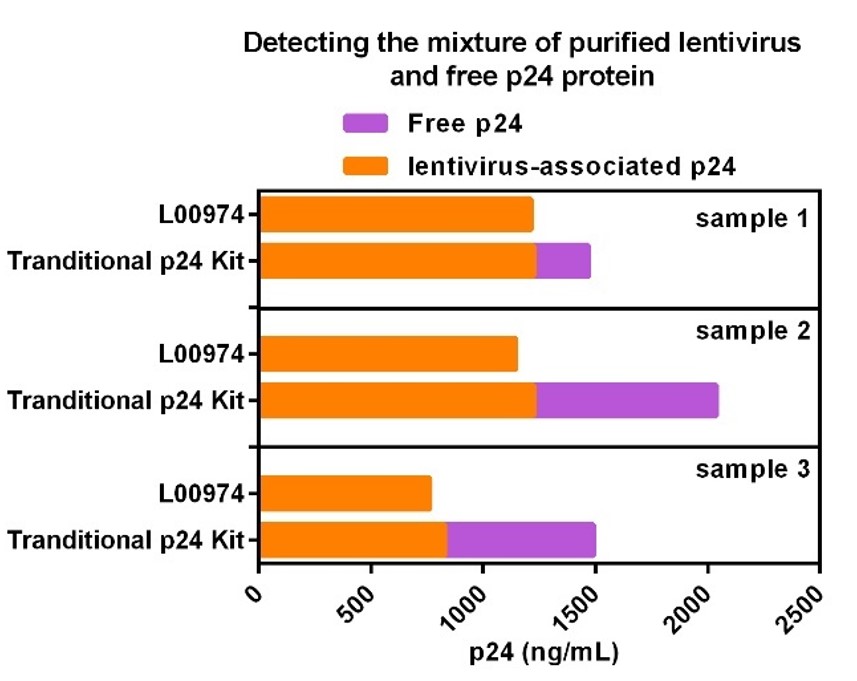
图4:特异性检测慢病毒颗粒上的p24蛋白
将不同浓度的p24蛋白添加到纯化的慢病毒样本中,结果显示,Lentivirus Titer p24 ELISA Kit Pro (GenScript, L00974),检测到的p24蛋白浓度与实际慢病毒颗粒上p24浓度一致。
回收率用于确定分析物检测是否受样品基质差异的影响,通过将已知量的分析物加标到不同的样品基质中来验证回收率。以下是根据具有代表性的准确度验证生成的报告和数据示例,在这项验证中,使用3批次试剂盒(GenScript, L00938),将已知量的分析物加标到基质中混合验证回收率,样本重复测量3次。
Table 1: 三批次试剂盒回收率测试结果为 86%-108%
| 批次编号 | 重复次数 | 平均测值(pg/mL) | 回收率 |
|---|---|---|---|
| #1 | 3 | 1945.30 | 86% |
| #2 | 3 | 1787.64 | 108% |
| #3 | 3 | 1752.76 | 90% |
A. 批内精密度/重复性
批内精密度验证体现测定板内每孔之间的重复性,有助于确保在测定板的不同孔中运行样本检测可以给出可靠的结果。 以下是根据具有代表性的批内精密度验证生成的报告和数据示例,在这项验证中,使用金斯瑞p24检测试剂盒(GenScript, L00938),分别对低、中、高3个浓度水平的样本进行测试,每个样本各重复检测10次,每个样本计算10次测量浓度结果的变异系数(CV)。
Table 2: 三批次试剂盒批内精密度验证结果
| 批次编号 | 重复次数 | 平均测值(pg/mL) | %CV |
|---|---|---|---|
| #1 | 10 | 215.55 | 3% |
| #1 | 10 | 829.45 | 4% |
| #1 | 10 | 1537.42 | 4% |
| #2 | 10 | 209.60 | 5% |
| #2 | 10 | 792.76 | 2% |
| #2 | 10 | 1431.42 | 3% |
| #3 | 10 | 188.09 | 6% |
| #3 | 10 | 759.99 | 4% |
| #3 | 10 | 1377.71 | 3% |
B. 批间精密度
批间精密度体现同一样品在多批测定间的重现性,有助于确保在不同批次试剂盒中运行样本检测可以给出可靠的结果。 以下是根据具有代表性的批间精密度验证生成的报告和数据示例,在这项验证中,使用3个不同批次试剂盒(GenScript, L00938),分别对低、中、高3个浓度水平的样本进行测试,每个样本各重复检测10次,每个样本计算30次测量浓度结果的变异系数(CV)。
Table 3: 三批次试剂盒批间差验证结果
| 批次数量 | 重复次数 | 平均测值 pg/mL | %CV |
|---|---|---|---|
| 3 | 3×10 | 204.41 | 7% |
| 3 | 3×10 | 794.07 | 5% |
| 3 | 3×10 | 1448.85 | 6% |
病毒滴度有两种表示方式:以转导测量的功能(传染性)滴度或以病毒颗粒测量的物理滴度。物理滴度是测量样本中存在多少病毒,通常根据蛋白质(例如p24)的水平计算。功能滴度是衡量有多少病毒可以感染细胞的指标,通常比物理滴度低 100-1000 倍。
对于Lentivirus Titer p24 ELISA Kit (GenScript, L00938),可以使用试剂盒中稀释后的1× Wash Solution进行样本稀释,效果是相同的。 对于Lentivirus Titer p24 ELISA Kit Pro (GenScript, L00974),在分离游离p24阶段,可以不对慢病毒上清样本进行稀释;若稀释,则使用Cell culture medium(10% FBS);在后续的ELISA检测阶段,可以使用试剂盒中稀释后的1× Wash Solution稀释。如果使用样本或制剂buffer作为标准品和样品的稀释液,需要通过预实验测试回收率是否符合预期,符合预期则可以使用,否则不建议使用。其他稀释液例如超纯水,未添加FBS的DMEM等都不能保证正常输出结果。如果您需要验证方面的支持,可以联系我们。 对于Lentivirus Titer p24 Kit Easy (GenScript, L01019),推荐使用 Assay Dilution Buffer(GenScript, B00062)。自行配制推荐配方为 1×PBS,10% FBS,1‰ Tween 20。
Lentivirus Titer p24 ELISA Kit Pro 仅会检测出慢病毒衣壳中的p24蛋白,不会检测出游离的p24蛋白,通过ELISA方法测定,全程耗时约3 h。
Lentivirus Titer p24 ELISA Kit 检测的是总p24蛋白,包括游离的p24蛋白和慢病毒衣壳中的p24蛋白,通过ELISA方法测定,全程耗时约2.5 h。
Lentivirus Titer p24 ELISA Kit Easy 检测的是总p24蛋白,通过化学放光法进行测定,孵育时间为15分钟,检测过程无需洗涤,全程耗时约30分钟。
均不含有人源材料,生物风险低。
Lentivirus Titer p24 ELISA Kit (GenScript, L00938),Lentivirus Titer p24 ELISA Kit Pro (GenScript, L00974) 试剂盒中各配有一块预包被的96孔酶标板,其中包含8 孔 x 12 板条,我们建议按照说明书中推荐的标准曲线稀释梯度,配置8个标准品工作液。 为了确保滴度的可靠定量,建议标准品和样品均一式两份进行重复测试。由此可计算出一个试剂盒可以测试40个样本。
Lentivirus Titer p24 Kit Easy (GenScript, L01019) 所提供的试剂可按照说明书建议的工作体积进行96次测定。如果使用384孔板进行测定,所用试剂体积可进行等比例减少,但需要进行预实验确定测定的可靠性。
本品不固定检测板型号,客户可自行选择合适的检测板,以下为选择指南:
无效。需要调整稀释倍数重新复测。
慢病毒滴度p24检测试剂盒均为25℃反应,不会出现边缘效应。
可单独选购 20× Wash Solution (GenScript, B00063),该洗液适用于 Lentivirus Titer p24 ELISA Kit (GenScript, L00938),Lentivirus Titer p24 ELISA Kit Pro (GenScript, L00974) 。
Lentivirus Titer p24 ELISA Kit Pro, Lentivirus Titer p24 ELISA Kit 需使用能测定 450 nm 吸光度的酶标仪。酶标仪通过检测酶标板中液体的吸光值,读取OD值后进行定性或定量分析。
Lentivirus Titer p24 ELISA Kit Easy 需使用能进行化学发光检测的微孔板读数仪/读板机/酶标仪/分析仪。化学发光分析仪通过光电倍增管将化学发光反应(酶促发光或直接发光)产生的光信号转换为相应的信号值,用RLU(相对光单位)表示,以达到定量或定性的检测目的。
参考文献
| 产品编号 | 名称 | 数量 | 价格 | 操作 |
|---|---|---|---|---|
|
B00062
|
Assay Dilution Buffer |
|
¥651.00 60 mL |
|
|
B00063
|
20× Wash Solution |
|
¥498.00 60 mL |
|
|
D00042
|
96-well Low Binding White Microplates & Sealers |
|
¥698.00 5 plates |
|
|
L00350
|
ToxinSensor™ Chromogenic LAL Endotoxin Assay Kit |
|
¥800.00 |
|
|
L00351
|
ToxinSensor™ Gel Clot Endotoxin Assay Kit |
|
¥1250.00 1 Kit |
|
|
L00886
|
Benz-Neburase™ Nuclease ELISA Kit |
|
¥7200.00 96 Tests |
|
|
L00942
|
AAV2 Titer Capsid ELISA Kit |
|
¥4980.00 96 Tests |
|
|
L00976
|
BSA ELISA Kit, 2G |
|
¥4980.00 96 Tests |
|
|
L01041
|
MuLV Titer p30 ELISA Kit |
|
¥9800.00 96 Tests |
|
|
Z03695
|
Benz-Neburase™, tag-free |
|
¥392.00 |
|
|
Z03708
|
Benz-Neburase™ GMP, tag free |
|
¥2100.00 |
|
